Atomística
Filosofia
Demócrito e Leucipo entendiam que
dividindo a matéria de forma recur-
siva, chegariam um ponto em que a
divisão seria impossível, o Átomo
Científico
Dalton
O átomo era uma partícula
indivisível, maciça e neutra

- Em uma reação química
nenhum átomo é criado ou
destruído
- Cada elemento tem um á-
tomo de massa e tamanho
específico
- A combinação de átomos
diferentes em uma propor-
ção de números inteiros ge-
ra uma substância diferente
Descoberta do Elétron por meio do experimento de raios catódicos
Thomson
Experimento da colisão de partículas alfa mostra que existe um espaço vazio no átomo
Rutherford
O átomo é formado por um núcleo
de prótons de carga negativa. Em
torno desse núcleo, os elétrons per-
formavam órbitas criculares.
A hipótese de Rutherfrod foi contestada pois as partículas negativas deveriam ser atraídas pelo núcleo positivo até se chocarem
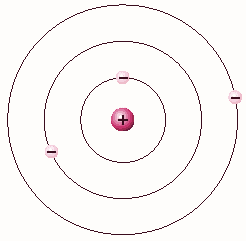
Bohr
Na tentativa de provar a hipóstese
de Thomson, Bohr cria seus postu-
lados.
- A órbita dos elétrons é dividida
em 7 camadas: K,L,M,N,O,P,Q.
- A energia do elétron é quantiza-
da, ou seja, cada camada tem uma
energia definida.
- Se um elétron é excitado e salta
uma camada, este liberará a ener-
gia em froma de onda eletromag-
nética.
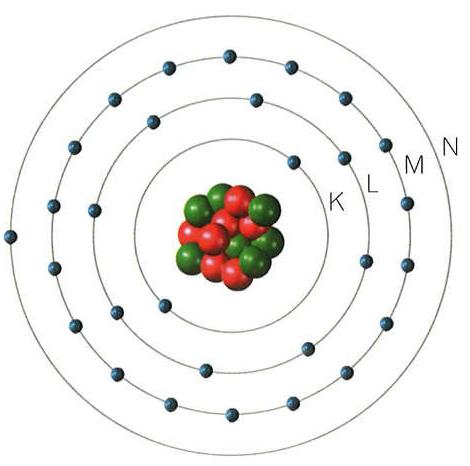
Modelo atômico Clássico
Modelo atômico de Thompson, mais os nêutrons, órbita elíptica dos elétrons e postulados de Bohr.
O átomo era formado por uma massa
positiva e era envolta pelos elétrons

