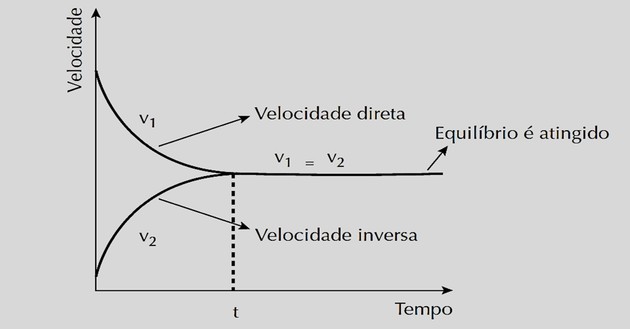
Equilíbrio químico
O equilíbrio químico ocorre quando, em uma reação reversível, a velocidade da reação direta é igual à velocidade da reação inversa. Uma vez atingido o estado de equilíbrio, as concentrações de reagentes e produtos permanecem constantes.
Constante de equilíbrio em função da concentração

Sólidos e líquidos não podem ser usados na fórmula do Kc
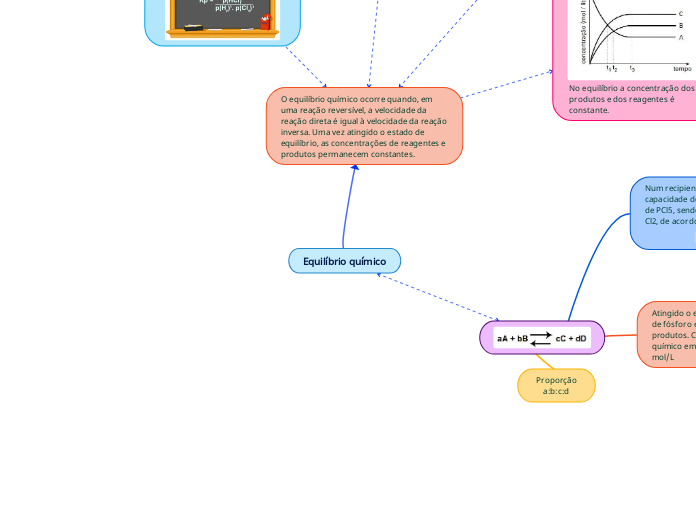
Constante de equilíbrio em função da pressão
Válido apenas para gases
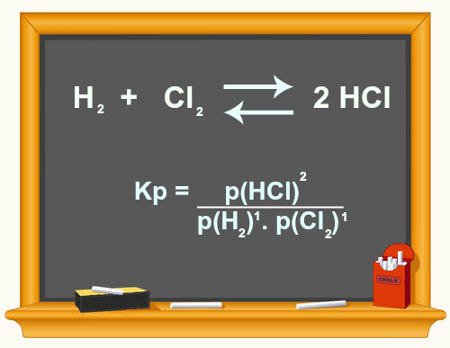
Gráfico reação com equilíbrio

No equilíbrio a concentração dos produtos e dos reagentes é constante.
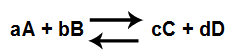
Num recipiente de paredes rígidas e com capacidade de 2,0 L, foram aquecidos 2,0 mol de PCl5, sendo este decomposto em PCl3 e Cl2, de acordo com a seguinte equação:

Atingido o equilíbrio químico, o pentacloreto de fósforo estava 40% dissociado em seus produtos. Calcule a constante de equilíbrio químico em função das concentrações em mol/L
Primeiramente vamos considerar que a concentração de PCl5 no início do experimento era de 1,0 mol/L e em seguida passamos para a montagem da tabela (início / reage / equilíbrio). Note que já sabemos o quanto de PCl5 foi consumido através do valor do grau de equilíbrio de 40%.

Reagentes
equilíbrio=início-reage
Produtos
equilíbrio=forma

Com os valores das concentrações dos componentes do equilíbrio podemos agora calcular a constante de equilíbrio.